|
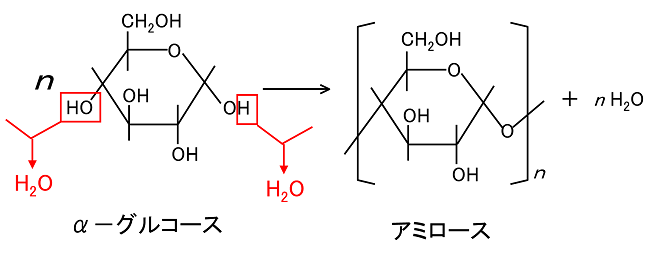
�R�@�������� �y�V�R�����q�������z �@��ʂɁC���q�ʂ�10000����悤�ȕ����������q�������Ƃ����B�����̍����q�������́C�����̕��q�ʂ̏����ȕ��q���k�@�t���@�l��k�@�k���@�l�ɂ���ďd�����C���̂���Ԃ��P�ʂ��������������\�����Ƃ��Ă���B���̒ᕪ�q���k�@�P�ʑ��@�l�܂��́k�@���m�}�[�@�l�C�������鍂���q���k�@�d�����@�l�܂��́k�@�|���}�[�@�l�Ƃ����B�Ⴆ�C�f���v���̓�-�O���R�[�XC6H12O6���P�ʑ̂ƂȂ�CH2O���Ƃ�ďk���d���������̂ł���B���̂��߁CC6H10O5
�̂���Ԃ��\���ƂȂ�(C6H10O5)n�ƕ\�����B����n���k�@�d���x�@�l�Ƃ����B |
|
 |
|
|
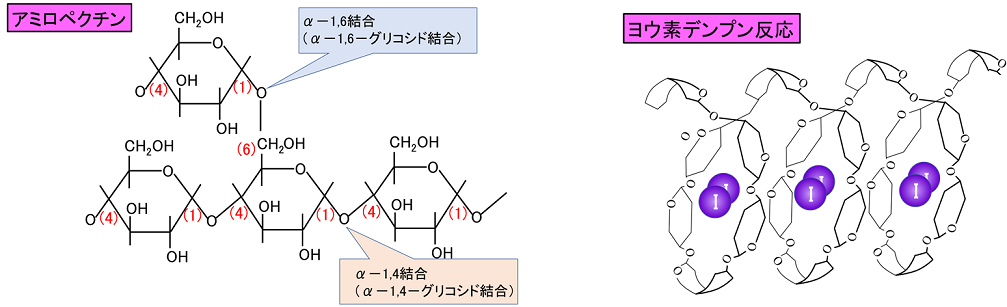
�����q�������͒ᕪ�q�������ƈقȂ�C�������q���ŕ\����镨���ł��C�d���x���قȂ���̂��W�܂��Ă���̂ŁC�Z�_�Ȃǂ͖��m�Ȓl�������Ȃ��B���q�ʂ͕��ϒl�i���ϕ��q�ʁj�ŕ\������B �@�܂��C�����Ȓᕪ�q�������͕��q���K���������z�Č����ƂȂ邪�C�����q�������͕��q�S�̂��K���������z�邱�Ƃ͂Ȃ��C�K���������z�������i�����̈�j�ƕs�K���ɂȂ��Ă��镔���i���̈�j�����荬�������\���ƂȂ��Ă����B �@�����q��������1�̕��q�ł��R���C�h���q�̑傫���i���a10�|9�`10�|7m�j�ɂȂ���̂������C��ʂɗn�}�ɂ͗n�����Ȃ����C�R���C�h�n�t�i�R���C�h���q���n�}�ɕ��U���Ă����ԁj�ɂȂ邱�Ƃ������B �y�����ށz �@����̒P�����E���k���ɂ���āC���������������̂������ł���B�k�@�f���v���@�l��k�@�Z�����[�X�@�l�Ȃǂ�����C���̓��ɑ������݂��Ă���B�����͒P���̂փ~�A�Z�^�[���\�����Ȃ��̂ŁC�k�@�Ҍ����@�l�������Ȃ��B �y�f���v���z�@ �f���v���̍\�� �f���v��(C6H10O5)n�@�͑����́k�@���|�O���R�[�X�@�l���k���������̂ŁC�ĂȂǂ̍����ɑ����܂܂�Ă���B�f���v���ɂ́k�@�A�~���[�X�@�l�Ɓk�@�A�~���y�N�`���@�l������B�A�~���[�X����-�O���R�[�X��1�ʂ�4�ʂ̒Y�f���q�ɂ�OH�Ō������C������Ɍ�������B ����C�A�~���y�N�`������-�O���R�[�X�̒����̂Ƃ���ǂ���Ɏ}�����ꂪ������B����́C�Ƃ���ǂ������-�O���R�[�X��1�ʂ�6�ʂ̒Y�f���q�ɂ�OH�ŏk�����邽�߂ł����B �ʏ�̕Ă̓A�~���[�X��20�`25���܂܂�C�����Ă̓A�~���y�N�`����100���ł���B |
|
 |
|
|
���E�f�f���v������ �f���v���̓O���R�[�X6�ň��]����悤�ȁC�k�@�点���@�l�\�����Ƃ��Ă���C���̌`�͕��q���́|OH�Ԃɐ�����k�@���f�����@�l�ɂ���ĕێ�����Ă���B �f���v���̐��n�t�Ƀ��E�f�n�t��������ƁC�f���v�����q�̂点��\���̒���I2���q�����荞�݁C�`���F��悷��i�E��j�B���̔��������E�f�f���v�������Ƃ����B�点�����\�������Ă�����̂قǂ�葽����I2���q�����荞�ށB��F�͓��荞��I2���q�������Ȃ�ɂ�C�ԁ��Ԏ��������ƕω�����B�A�~���[�X�͂点�����̂ŔZ���ɂȂ邪�C�A�~���y�N�`���͎}�����ꂪ���邽�߁C�点��͒Z���Ȃ�̂Ő��`�Ԏ��ɂȂ�B�O���R�[�Q���͐Ԋ��F�ɂȂ�B ���E�f�f���v�������̒�F�́C���M����ƃf���v���̂点��\����������邽�߁C���荞��ł���I2���q�������̂ŐF����������B��₷�ƍĂь������ĐF�����B �������� �f���v��(C6H10O5)n�Ɋ_��_�Ȃǂ���p������ƁC�f���v�������d���x�̒Ⴂ�k�@�f�L�X�g�����@�l(C6H10O5)n�f �in��n�f�j���o�ăO���R�[�X�܂ŕ��������B�y�f�k�@�A�~���[�[�@�l����p������ƁC�f�L�X�g�������o�āk�@�}���g�[�X�@�l�܂ŕ��������B�@ |
|
 |
|
|
�y�Z�����[�X�z �Z�����[�X(C6H10O5)n�@�͑����́k�@���|�O���R�[�X�@�l��1�ʂ�4�ʂ̒Y�f���q��OH�ŏk���������̂ŁC�A���זE�̍זE�ǂ̎听���ł���B���₻�̑��̗n�}�ɗn���ɂ����C�@�ۂƂ��ė��p������B�Z�����[�X�ׂ͗荇���O���R�[�X���q�̏㉺���t�ɂȂ�C�点��\�����Ƃ炸�C������ɂȂ�B���̂��߁C�Z�����[�X�̓��E�f�f���v�������������Ȃ��B�܂��C���s�ɕ��������q�Ԃɂ�OH�ɂ��k�@���f�����@�l�������邽�߃Z�����[�X�͏�v�ȑ@�ۂɂȂ�B �Z�����[�X�͍y�f�k�@�Z�����[�[�@�l�ɂ���āC�́k�@�Z���r�I�[�X�@�l�܂ŕ��������B |
|
 |
|
|
�y�Z�����[�X�̗U���́z �Z�����[�X(C6H10O5)n�@��1�̃O���R�[�X�̒P�ʂɃq�h���L�V�3����̂ŁC�k�@[C6H7O2(OH)3]n�@�l�̂悤�ɕ\�����Ƃ�����B����3�̃q�h���L�V���F�X�ȍ\���ɕω������邱�Ƃɂ��C�L�p�ȕ��������邱�Ƃ��ł���B �j�g���Z�����[�X �@�Z�����[�X�i�ȁC�p���v�j�Ɂk�@�Z�Ɏ_�@�l�Ɓk�@�Z���_�@�l�̍����n�t�i���_�j����p������ƁC�Z�����[�X�̃q�h���L�V��|OH���Ɏ_�G�X�e���|ONO2�ƂȂ�B���ꂪ�j�g���Z�����[�X�ł���B [C6H7O2(OH)3]n�@�{�@3nHNO3�@���@[C6H7O2(ONO2)3]n�@�{�@3nH2O |
|
 |
|
| �@�j�g���Z�����[�X�̒��f�̊����i���ʁ��j���ɉ��x�Ƃ����C�g���j�g���Z�����[�X[C6H7O2(ONO2)3]n�ł�14.1���C�W�j�g���Z�����[�X[C6H7O2(OH)(ONO2)2]n�ł�11.1���ƂȂ�B�j�g���Z�����[�X�͏ɉ��ȂƂ��C�ɉ��x��13��������̂����Ȗ�Ƃ����C�g���j�g���Z�����[�X�͋��Ȗ�ƂȂ�B���Ȗ�͓_����Əu���ɔR�Ă��邽�߁C�����Ζ�̌����ƂȂ�B
�ɉ��x10�`13���̃j�g���Z�����[�X����Ȗ�Ƃ����B�W�j�g���Z�����[�X�͎�Ȗ�̎听���ƂȂ�B��Ȗ���G�^�m�[���ɗn���������̂� �R���W�I���Ƃ����C�n�}��������������ɂ������͓̂��͖��Ɏg����B����ɏɉ��x�����������̂͐ƖȖ�Ƃ��C�Y�܁i�_������������܁j�ƍ������荇�킹��������̂��̂̓Z�����C�h�Ƃ���B�Z�����C�h�́C���Ă͕��[��C�ߋ�C�f��t�B�����ȂǂȂǗl�X�ȗp�r�����������C�R���₷���Ƃ������_������C���݂ł͐Ζ��n�v���X�`�b�N�Ɏ���đ����Ă���B
�Đ��@�ہi���[�����j �Z�����[�X�����w�����ň�x�n����C�������Đ������@�ۂɂ������̂��k�@�Đ��@���@�l�Ƃ����C�Z�����[�X�̍Đ��@�ۂ��k�@���[�����@�l�܂��͐l�������Ƃ����B���[�����ɂ̓r�X�R�[�X���[�����Ɠ��A�����j�A���[����������B �Z�����[�X��Z�����_���i�g���E���Ɠ��Y�fCS2�ŏ�������ƐԊ��F�����̃R���C�h�n�t���ł���B������k�@�r�X�R�[�X�@�l�Ƃ����B�r�X�R�[�X���_���ɍE���牟���o���Ƒ@�ۏ�ɋÌł���Ƌ��ɃZ�����[�X���Đ����đ@�ۂ�������B���̑@�ۂ��k�@�r�X�R�[�X���[�����@�l�Ƃ����B�܂��C�r�X�R�[�X��ɍĐ��������̂��@�k�@�Z���n���@�l�Ƃ����B ���_����(�U)Cu(OH)2��Z�A�����j�A���ɗn�������[�F�n�t�iCu(OH)2�{4NH3��[Cu(NH3)4]2�{�{2OH�|�j���k�@�V���o�C�c�@�[�����@�l�Ƃ����B�Z�����[�X���V���o�C�c�@�[����ɗn�����ƔS���̂���t�̂�������B���̗n�t���E����_���ɉ����o���ƃZ�����[�X���Đ����đ@�ۂ�������B���̑@�ۂ��k�@���A�����j�A���[�����@�l�܂��́k�@�L���v���@�l�Ƃ����B �������@�ہi�A�Z�e�[�g�j �Z�����[�X�ɐ|�_�i�n�}�j�Ɩ����|�_
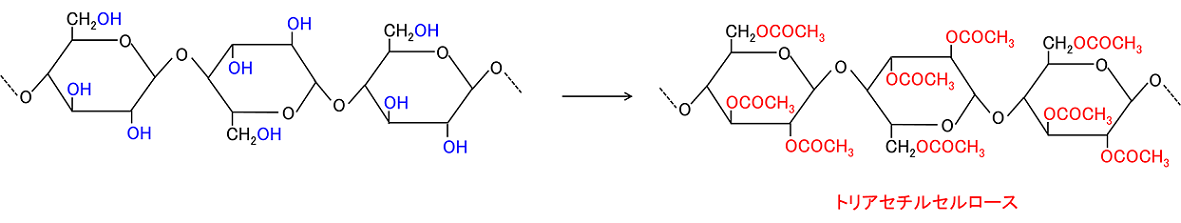
(CH3CO)2����я��ʂ̔Z���_�i�G�}�j����p������ƁC�Z�����[�X���̃q�h���L�V��G�X�e�����i-OH��H���A�Z�`����CH3CO-�ƒu�������C-OCOCH3�ƂȂ�j����āk�@�g���A�Z�`���Z�����[�X�@�l���ł���B�g���A�Z�`���Z�����[�X�͕��q����OH����S�ɃG�X�e�����i�A�Z�`�����j����Ă��邽�ߗn�}�ɗn���ɂ����B�����ŁC����������50��C
�ɕۂƁC�G�X�e���̈ꕔ��������������āC�A�Z�g���ɉn�ȁk�@�W�A�Z�`���Z�����[�X�@�l��������B���̃A�Z�g���n�t���E�����C���ɉ����o���Ċ�������Ɓk�@�A�Z�e�[�g�@�l�Ƃ����@�ۂ�������B�A�Z�e�[�g�̂悤�ɓV�R�@�ۂ����H�������̂��k�@�������@���@�l�Ƃ����B �@[C6H7O2(OH)3]n�@�{�@3n(CH3CO)2�@���@[C6H7O2(OCOCH3)3]n�@�{�@3nCH3COOH |
|
 |
|
|
[C6H7O2(OCOCH3)3]n�@�{�@nH2O�@���@[C6H7O2(OH)(OCOCH3)2]n�@�{�@nCH3COOH |
|
 |
|
|
����@���̊e�₢�ɓ�����BH��1.0�CC��12�CO��16�CCu��64 (1)�@�f���v��32.4g�����ׂă}���g�[�X�܂łɂ���ƁC������}���g�[�X�͉�g���B (2)�@���q�ʂ�2.43�~105�̃A�~���[�X���̃O���R�[�X�P�ʂ̌��͂����炩�B (3)�@�X�N���[�X1.71g�𐅂ɗn�����C�y�f��p���ĉ������������B���̔����t�ɉߏ�̃t�F�[�����O�t�������Ĕ����������Ƃ���C�_����(�T)�̒��a��0.409g�������B1mol�̒P������1mol�̎_����(�T)������������̂Ƃ��āC�X�N���[�X�̉�%�������������ꂽ�����߂�B (4)�@�A�Z�e�[�g�@��41g�����邽�߂ɂ́C���Ƃ̃Z�����[�X����g�K�v���B (5)�@8.1g�̃Z�����[�X�����S�ɃA�Z�`��������̂ɕK�v�Ȗ����|�_�̎��ʁkg�l�C����ѓ�����g���A�Z�`���Z�����[�X�̎��ʁkg�l���C�L������2���ŋ��߂�B (6)�@�A�~���[�X���_�ƂƂ��ɒZ���ԉ��M���ĕ����I�ɉ����������C���q��1.62�~103�̓����B���̓��́C�����q�̃O���R�[�X�������������̂��B�܂��C���̓��ɖ����|�_����p�����āC�|OH�̑S�Ă��A�Z�`���������B�A�Z�`�������ꂽ���̕��q�ʂ́C���Ƃ̓��ɔ�ׂ����瑝���������B (1)�@[C6H10O5]n�@�{�@n/2H2O�@���@n/2C12H22O11�@���C�f���v��1mol�i��162n�kg�l�j����}���g�[�Xn/2mol�i��342�~n/2�kg�l�j������B�f���v��32.4g�ł́C342�~n/2�~(32.4/162n)��34.2�kg�l (2)�@�A�~���[�X��[C6H10O5]n�Ȃ̂ŁC���q�ʂ�162n�B����āC2.43�~105��162n���Cn��1.5�~103�k�l (3)�@�X�N���[�X1mol����P��2mol������B�܂��C1mol�̒P������1mol��Cu2O����������̂ŁC�����ʁkmol�l�̗ʓI�W�́C������Cu2O�����������P����2�~(���������X�N���[�X)�ƂȂ�B���������X�N���[�X�́C(0.409/144)/2�kmol�l�B��������ʁkg�l�ɂ���ƁC(0.409/144)/2�~342�kg�l�B���������X�N���[�X�́��́C(0.409/144)/2�~342/1.71�~100��28.4��28�k���l�B (4)�@[C6H7O2(OH)3]n��[C6H7O2(OH)(OCOCH3)2]n�̕ω��Ȃ̂ŁC�Z�����[�X1mol�i��162n�kg�l�j����A�Z�e�[�g1mol�i��246n�kg�l�j��������B�A�Z�e�[�g41g������ɕK�v�ȃZ�����[�X�́C162n�~(41/246n)��27�kg�l (5)�@[C6H7O2(OH)3]n�{3n(CH3CO)2��[C6H7O2(OCOCH3)3]n�{3nCH3COOH�Ȃ̂ŁC�Z�����[�X1mol�i��162n�kg�l�j�Ɩ����|�_3n mol�i��3n�~102�kg�l�j����������̂ŃZ�����[�X8.1g�ł́C3n�~102�~(8.1/162n)��15.3��15�kg�l�B�܂��C�Z�����[�X1mol�i��162n�kg�l�j����g���A�Z�`���Z�����[�X1mol�i��288n�kg�l�j������̂ŁC�Z�����[�X8.1g�ł́C288n�~(8.1/162n)��14.4��14�kg�l (6)�@�A�~���[�X�������������Đ�����f�L�X�g����[C6H10O5]n���l����B���̃f�L�X�g�����̕��q�ʂ�162n�Ȃ̂ŁC162n��1.62�~103���Cn =10.0�kmol�l�B�܂��C�A�Z�`���������[C6H7O2(OH)3]10��[C6H7O2(OCOCH3)3]10�̕ω��Ȃ̂ŕ��q�ʂ̕ω��́C288�~10�|1.62�~103��1.26�~103�B |
|
 |
